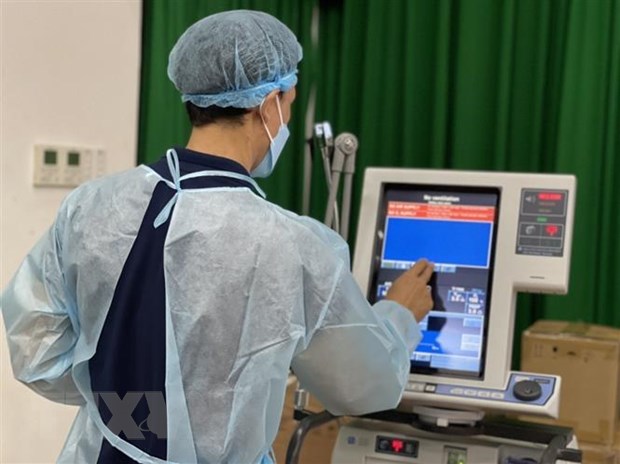
Thiết bị y tế tại Bệnh viện Đa khoa Thống Nhất (tỉnh Đồng Nai). (Ảnh: TTXVN phát)
Tại Thông tư 13/2021/TT-BYT ban hành ngày 16-9 về quy định cấp số lưu hành, nhập khẩu trang thiết bị y tế phục vụ phòng, chống dịch COVID-19 trong trường hợp cấp bách, Bộ Y tế đưa ra điều kiện áp dụng hình thức cấp số lưu hành cho trang thiết bị y tế phòng dịch COVID-19.
Cụ thể, Điều 2 Thông tư 13/2021 nêu rõ trang thiết bị y tế được áp dụng hình thức cấp nhanh số lưu hành nếu đáp ứng đồng thời các điều kiện sau:
Thuộc danh mục 17 trang thiết bị sau: máy tách chiết; máy PCR; hóa chất (sinh phẩm) chạy máy PCR xét nghiệm SARS-CoV-2; test kít xét nghiệm nhanh kháng nguyên/ kháng thể kháng SARS-CoV-2; máy thở chức năng cao, máy thở xâm nhập và không xâm nhập, máy thở không xâm nhập, máy oxy dòng cao, máy thở xách tay; máy lọc máu liên tục; máy X-Quang di động; máy siêu âm Doppler màu ≥ 3 đầu dò; máy đo khí máu (đo được điện giải, lactat, hematocrite); máy theo dõi bệnh nhân ≥ 5 thông số; bơm tiêm điện; máy truyền dịch; máy phá rung tim có tạo nhịp; máy điện tim ≥ 6 kênh; máy siêu âm xách tay; máy đo thời gian đông máu; máy đo huyết động.
Thuộc một trong các trường hợp:
Đã được một trong các tổ chức sau cho phép lưu hành hoặc sử dụng khẩn cấp: Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA)-Mỹ; Cục Quản lý hàng hóa trị liệu (TGA)-Australia; Cơ quan quản lý y tế Canada (Health Canada)...
Đã được cơ quan có thẩm quyền của các nước thuộc khu vực châu Âu gồm: Áo; Ba Lan; Bồ Đào Nha; Bulgaria; Croatia; Estonia; Hungary; Hy Lạp; Ireland; Latvia; Đức; Litva; Malta; Phần Lan; Pháp; Romania; Séc; Síp; Slovakia; Slovenia; Tây Ban Nha; Italy; Luxembourg; Thụy Sỹ; Anh; Bỉ; Đan Mạch; Hà Lan; Thụy Điển cho phép lưu hành, sử dụng khẩn cấp.
Thuộc danh mục sản phẩm xét nghiệm COVID-19 được sử dụng khẩn cấp do Tổ chức Y tế thế giới (WHO) công bố trên trang web tại địa chỉ https://extranet.who.int.
Thuộc danh mục các sản phẩm phổ biến để xét nghiệm COVID-19 do Ủy ban an ninh y tế của châu Âu ban hành công bố trên trang web tại địa chỉ https://ec.europa.eu.
Đã được cấp giấy phép nhập khẩu theo hình thức thương mại tại Việt Nam trước ngày 16-9-2021.
Được sản xuất trong nước theo hình thức chuyển giao công nghệ, hình thức gia công đối với trang thiết bị y tế thuộc một trong các trường hợp nêu trên.
Cũng tại Thông tư này, Bộ Y tế nêu rõ giá trị của số lưu hành: số lưu hành được cấp theo quy định tại Thông tư này có hiệu lực kể từ ngày ký ban hành đến ngày 31/12/2022.
Bộ Y tế cũng nêu rõ trang thiết bị y tế chưa có số lưu hành nhập khẩu để phục vụ phòng, chống dịch COVID-19 với mục đích viện trợ phải được cơ quan có thẩm quyền phê duyệt theo quy định hiện hành của pháp luật về quản lý và sử dụng viện trợ nước ngoài.
Việc thông quan phải căn cứ theo quyết định tiếp nhận viện trợ của cơ quan có thẩm quyền và không cần giấy phép nhập khẩu trang thiết bị y tế của Bộ Y tế./.
Theo Minh Huệ (TTXVN/Vietnam+)
























![[Video] Bộ Y tế yêu cầu bảo đảm cấp cứu người bệnh trong 2 kỳ nghỉ lễ [Video] Bộ Y tế yêu cầu bảo đảm cấp cứu người bệnh trong 2 kỳ nghỉ lễ](https://images.baoangiang.com.vn/image/news/2026/20260426/thumbnail/510x286/-video-bo-y-te-yeu-_2996_1777187762.jpg)









 Đọc nhiều
Đọc nhiều








![[Video] Bộ Y tế yêu cầu bảo đảm cấp cứu người bệnh trong 2 kỳ nghỉ lễ [Video] Bộ Y tế yêu cầu bảo đảm cấp cứu người bệnh trong 2 kỳ nghỉ lễ](https://images.baoangiang.com.vn/image/news/2026/20260426/thumbnail/336x224/-video-bo-y-te-yeu-_2996_1777187762.jpg)



![[Video] Hơn 500.000 thí sinh chưa đăng ký thi tốt nghiệp THPT 2026 [Video] Hơn 500.000 thí sinh chưa đăng ký thi tốt nghiệp THPT 2026](https://images.baoangiang.com.vn/image/news/2026/20260426/thumbnail/336x224/-video-hon-500-000-_8314_1777166269.jpg)
